Reaktionsgleichung
Hinweis
Es wird darauf hingewiesen, dass für jedes Experiment entsprechend der eigenen Durchführung vor der erstmaligen Aufnahme der Tätigkeit eine Gefährdungsbeurteilung durchgeführt und dokumentiert werden muss. Jede fachkundige Nutzerin/jeder fachkundige Nutzer muss die aufgeführten Inhalte eigenverantwortlich prüfen und an die tatsächlichen Gegebenheiten anpassen.
Weder die Redaktion des Lehrerfortbildungsservers noch die Autorinnen und Autoren der veröffentlichten Experimente übernehmen jegliche Haftung für direkte oder indirekte Schäden, die durch exakten, veränderten oder fehlerhaften Nachbau und/oder Durchführung der Experimente entstehen. Weiterführende Informationen erhalten Sie unter www.gefahrstoffe-schule-bw.de
Übung Verhältnisformel und Reaktionsgleichung
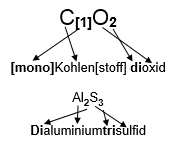
Für Metall-Nichtmetallverbindungen (z.B. NaCl) gilt:- Metalle stehen in der Formel und im Namen an 1. Stelle.
- Nichtmetalle erhalten meist die Endung -id. (z.B. -chlorid).
- Die Vorsilbe (z.B. Di, Tri …) im Namen gilt für das nachfolgende Element.
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
mono |
di |
tri |
tetra |
penta |
hexa |
hepta |
octa |
Beispiele:
(wird oft nicht angegeben)
Aufgabe 1
Gib den Namen/Formel der Teilchen an! Male dazu farbig die Atome als Kugeln.
|
MgO |
Magnesiumoxid
|
Dialuminiumtrioxid |
|
Siliciumdioxid |
|
|
Li 2 O |
|
Magnesiumdichlorid |
|
|
NO |
|
NO 2 |
|
Dilithiumsulfid |
|
Stickstoff |
|
|
CO |
|
Diphosphorpent(a)oxid |
|
Schwefeldioxid |
|
Aufgabe 2
Gib die Reaktionsgleichung an. Male dazu immer die Atome als Kugeln. (HEFT)
Reaktion
a) Kohlenstoff verbrennt (d.h. reagiert mit Sauerstoff) zu CO
2
.
b) Wasserstoff verbrennt zu
Wasser
.
c) Magnesium reagiert mit Chlor zu Magnesiumdichlorid.
d) Dieisentrioxid und Aluminium reagieren zu Eisen und Dialuminiumtrioxid
e) NH3 (
Ammoniak
) entsteht aus den Elementen.
f) Koks reagiert mit Dieisentrioxid zu Fe und Kohlenstoffdioxid
g) HCl
Salzsäure
wird aus den Elementen hergestellt.
h)
Calciumcarbonat
CaCO
3
zerfällt in CaO und
Kohlenstoffdioxid
.
i)
Methan
CH
4
verbrennt zu Wasser und CO
2
.
Aufgabe 3
Unterstrichene Moleküle müssen in die Vokabelliste!
Lösung
Übung Verhältnisformel und Reaktionsgleichung
Für Metall-Nichtmetallverbindungen (z.B. NaCl) gilt:- Metalle stehen in der Formel und im Namen an 1. Stelle.
- Nichtmetalle erhalten meist die Endung -id. (z.B. -chlorid).
- Die Vorsilbe (z.B. Di, Tri …) im Namen gilt für das nachfolgende Element.
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
mono |
di |
tri |
tetra |
penta |
hexa |
hepta |
octa |
Beispiele:
(wird oft nicht angegeben)
Aufgabe 1
Gib den Namen/Formel der Teilchen an! Male dazu farbig die Atome als
Kugeln
.
|
MgO |
Magnesiumoxid
|
Dialuminiumtrioxid |
Al 2 O 3 |
Siliciumdioxid |
SiO 2 |
|
Li 2 O |
Dilithiumoxid |
Magnesiumdichlorid |
MgCl 2 |
Stickstoffmonoxid |
NO |
|
NO 2 |
Stickstoffdioxid |
Dilithiumsulfid |
Li 2 S |
Stickstoff |
N 2 |
|
CO |
Kohlenstoffmonoxid |
Diphosphorpent(a)oxid |
P 2 O 5 |
Schwefeldioxid |
SO 2 |
Aufgabe 2
Gib die Reaktionsgleichung an. Male dazu immer die Atome als
Kugeln
. (HEFT)
Reaktion
a) Kohlenstoff verbrennt (d.h. reagiert mit Sauerstoff) zu CO2.
![]()
b) Wasserstoff verbrennt zu
Wasser
.
![]()
c) Magnesium reagiert mit Chlor zu Magnesiumdichlorid.
![]()
d) Dieisentrioxid und Aluminium reagieren zu Eisen und Dialuminiumtrioxid
![]()
e) NH3 (
Ammoniak
) entsteht aus den Elementen.
![]()
f) Koks reagiert mit Dieisentrioxid zu Fe und Kohlenstoffdioxid
![]()
g) HCl
Salzsäure
wird aus den Elementen hergestellt.
![]()
h)
Calciumcarbonat
CaCO3 zerfällt in CaO und
Kohlenstoffdioxid
.
![]()
i)
Methan
CH4 verbrennt zu Wasser und CO2.
![]()
Aufgabe 3
Markierte Molekule
müssen in die Vokabelliste!
reaktionsgleichung
herunterladen
[doc][40 KB]
reaktionsgleichung
herunterladen
[pdf][88 KB]
reaktionsgleichung_loesung
herunterladen
[doc][42 KB]
reaktionsgleichung_loesung
herunterladen
[pdf][94 KB]
