Übung 2
Infobox
Diese Seite ist Teil einer Materialiensammlung zum Bildungsplan 2004: Grundlagen der Kompetenzorientierung. Bitte beachten Sie, dass der Bildungsplan fortgeschrieben wurde.
Hinweis
Es wird darauf hingewiesen, dass für jedes Experiment entsprechend der eigenen Durchführung vor der erstmaligen Aufnahme der Tätigkeit eine Gefährdungsbeurteilung durchgeführt und dokumentiert werden muss. Jede fachkundige Nutzerin/jeder fachkundige Nutzer muss die aufgeführten Inhalte eigenverantwortlich prüfen und an die tatsächlichen Gegebenheiten anpassen.
Weder die Redaktion des Lehrerfortbildungsservers noch die Autorinnen und Autoren der veröffentlichten Experimente übernehmen jegliche Haftung für direkte oder indirekte Schäden, die durch exakten, veränderten oder fehlerhaften Nachbau und/oder Durchführung der Experimente entstehen. Weiterführende Informationen erhalten Sie unter www.gefahrstoffe-schule-bw.de
|
Üben mit Experimenten - Verschiedene Übungsformate
Exp.: Chromatografische Ermittlung der Indikatorfarbstoffe in Universalindikator-Lösung / Modellexperiment zum Ablauf einer chromatografischen Trennung |
Ü2
|
Die Zusammensetzung von Universalindikatorfarbstoffgemischen kann chromatografisch ermittelt werden. Damit wird die Methode der Chromatografie eingeübt. Ein Zusatzexperiment zeigt wiederum die Farbe der einzelnen Indikatorfarbstoffe bei verschiedenen pH-Werten.
Geräte und Chemikalien
| Chromatografiekammern mit Deckel | Unisol® |
| oder Standzylinder mit Abdeckglasscheibe | Methylrot-Lösung |
| Glaskapillaren | Phenolphthalein-Lösung |
| Lineal, weicher Bleistift |
Methylorange-Lösung
Bromthymolblau-Lösung |
Laufmittel:
Natronlauge (0,1 mol · L
-1
) und Methanol im Volumenverhältnis 10:1
DC-Platten Polygram® Cellulose
Nach Durchführung und Auswertung des Experiments können zwei noch feuchte DC-Platten in vorbereitete Glaszylinder mit NH 3 – bzw. HCl-Atmosphäre gehängt werden, um die Indikatorfarben in alkalischen und sauren Lösungen zu zeigen (rechte Abbildung).
Das Praktikum kann mit einer Übung zum chemischen Rechnen verknüpft werden (Herstellung von 100mL Natronlauge der angegebenen Stoffmengenkonzentration aus festem NaOH und Wasser).



Abb.: dünnschichtchromatografische Identifizierung von Indikatorfarbstoffen in Unisol®
Modellexperiment zur Verteilungschromatografie
Zum nachhaltigen Verständnis des Grundprinzips einer Verteilungschromatografie dient folgender Modellversuch, an dem 10-20 Personen an drei längs nebeneinander stehenden Tischen arbeiten können.
Vorbereitung:
- 10 Papierblätter A4 rot an der schmalen Seite nebeneinander legen („stationäre Phase“)
- 10 Papierblätter A4 blau bereithalten („mobile Phase“)
- 20 Lego Steine rot (Farbstoff 1, wandert schneller) und 20 Lego Steine grün (Farbstoff 2, wandert langsamer) auf das erste rote Papierblatt legen
Am Startpunkt liegen 40 „Farbstoff“-Lego-Steine auf der „stationären
Phase“ am Startpunkt.
Das erste blaue Papierblatt („mobile Phase“) erreicht den Startpunkt.
Jetzt werden die „Farbstoff“-Teilchen auf die Phasen am Startpunkt
verteilt, und zwar stationär/mobil im Verhältnis 1:3 (rote Steine) und 3:1 (grüne
Steine).
Es liegen also
auf dem ersten roten Blatt: 5 rote
Steine und 15 grüne Steine
und auf dem ersten blauen Blatt: 15 rote Steine und 5 grüne Steine.
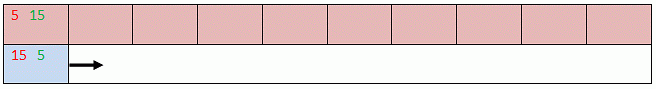
Jetzt „wandert“ die mobile Phase einen Ort weiter. Am Startpunkt
erscheint das nächste blaue Blatt.
Nun werden alle jeweils gegenüberliegenden Steine entsprechend des gegebenen
Verhältnisses neu verteilt.
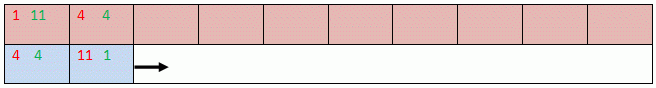
Das Prozedere wird wiederholt, bis die „Laufmittelfront“ am Ende
der „stationären Phase“ angekommen ist. Im Einzelfall muss beim
Verteilen um einen Stein gerundet werden.
ACHTUNG: Es müssen immer alle gegenüber zu liegen kommenden Steine neu verteilt
werden.
Es ergibt sich ein nachhaltiger Lerneffekt vom Grundprinzip der Verteilungschromatografie.
|
Üben mit Experimenten - Verschiedene
Übungsformate
|
Ü2 |
Zur nachhaltigen Darstellung der logarithmischen Skala der pH-Stufen (Verdünnung von Salzsäure bzw. Natronlauge mit je c=1 mol L -1 ) ist diese Verdünnungsreihe bestens geeignet.
Dabei wird mit einer 10mL-Spritze zügig von einem Becherglas zum nächsten verdünnt.
Salzsäure (ganz links stehend) 7x nach rechts
Natronlauge (ganz rechts stehend) 7x nach links
Geräte und Chemikalien
Becherglas 1,5 L, gefüllt mit Leitungswasser und zugesetztem Unisol®
Messzylinder 100 mL
15 Bechergläser 150 mL hohe Form
100 mL Salzsäure (c= 1mol · L
-1
)
100 mL Natronlauge (c= 1mol · L
-1
)
1 Medizintechnikspritze 10 mL
Dabei kann man zunächst nur die Salzsäure durchverdünnen (ab der Mitte ändert sich nichts mehr ???), und dann erst mit der Natronlauge zurück verdünnen. Auf die Art und Weise kann die Autoprotolyse des Wassers experimentell erarbeitet werden (Oxonium-Ionen müssen vom Wasser selbst gebildet werden, wenn sich ihre Konzentration durch Verdünnung nicht mehr ändert!)

Abb. Abschlussbild nach beiden Verdünnungsschritten
Aufgabe:
An diesem Experiment soll das Formulieren von begründeten Hypothesen geübt
werden.
Formulieren Sie entsprechende Arbeitsaufträge und Aufgaben.
Weiter zur Übung 3
