Thermolyse von Ammoniumchlorid
Infobox
Diese Seite ist Teil einer Materialiensammlung zum Bildungsplan 2004: Grundlagen der Kompetenzorientierung. Bitte beachten Sie, dass der Bildungsplan fortgeschrieben wurde.
Hinweis
Es wird darauf hingewiesen, dass für jedes Experiment entsprechend der eigenen Durchführung vor der erstmaligen Aufnahme der Tätigkeit eine Gefährdungsbeurteilung durchgeführt und dokumentiert werden muss. Jede fachkundige Nutzerin/jeder fachkundige Nutzer muss die aufgeführten Inhalte eigenverantwortlich prüfen und an die tatsächlichen Gegebenheiten anpassen.
Weder die Redaktion des Lehrerfortbildungsservers noch die Autorinnen und Autoren der veröffentlichten Experimente übernehmen jegliche Haftung für direkte oder indirekte Schäden, die durch exakten, veränderten oder fehlerhaften Nachbau und/oder Durchführung der Experimente entstehen. Weiterführende Informationen erhalten Sie unter www.gefahrstoffe-schule-bw.de
|
Exp.:
Übungen zu Protonenübergangsreaktionen |
Ü2
|
Unterrichtssituation (z.B. in Klasse 9):
Anhand von exemplarisch ausgewählten Reaktionen ist die Säure-Base-Reaktion als Protonenübergangsreaktion eingeführt. Die Fachbegriffe Säure als Protonenspender (-donator) und Base als Protonenempfänger (-akzeptor) sind etabliert. Konsequent wird die Teilchenebene betrachtet.
Das Wassermolekül wurde als amphoteres Teilchen diskutiert. Dabei ergibt sich
die Möglichkeit, die Oxonium-Ionen bzw. Hydroxid-Ionen als typische Teilchen
in sauren bzw. alkalischen Lösungen zu verstehen.
Häufig genutzte Experimente in diesem Unterrichtsgang sind:
- Reaktion von Chlorwasserstoff und Ammoniak, Bildung von Ammoniumchlorid-Rauch
- Überleiten von Chlorwasserstoff über Wasser, Leitfähigkeits- und pH-Messung
- Reaktion von Ammoniak mit Wasser, Ammoniak-Springbrunnen
Die wesentlichen Inhalte des Säure-Base-Konzepts entsprechend den Bildungsstandards für Klasse 10 sind in einem „Buddy Book“ zusammengestellt (siehe Material 4.4.1).
Zur Übung und Zusammenführung kann im weiteren Verlauf der Unterrichtseinheit ein Schülerpraktikum zur Thermolyse von Ammoniumchlorid durchgeführt werden, in dem die Stoffe Wasser, Ammoniak, Chlorwasserstoff und Ammoniumchlorid in vier verschiedenen Säure-Base-Reaktionen vorkommen. Dieses Praktikum eignet sich hier hervorragend zum Üben.
Es kann auch in der Kursstufe zur Wiederholung und Vertiefung des Säure-Base-Konzepts nach Brönsted verwendet werden.
Durchführung
Ein Löffelspatel Ammoniumchlorid wird in ein Reagenzglas gegeben.
Ein etwa 15 cm langer, mit Wasser angefeuchteter Streifen Universalindikatorpapier
wird in das Reagenzglas gelegt, so dass es vom Rand des Reagenzglases bis etwa
3 cm über die Ammoniumchloridportion reicht (oben leicht über den RGl-Rand klemmen).
In die Mitte des Reagenzglases wird mit der Pinzette ein Glaswollebausch gelegt.
Das Ammoniumchlorid wird vorsichtig mit der entleuchteten Brennerflamme erhitzt. Die Veränderungen am Universalindikatorpapier und an der Reagenzglaswand werden beobachtet.
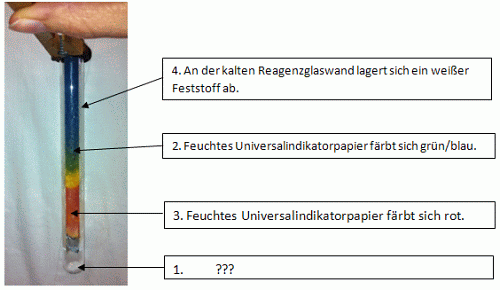
 Abb.: Versuchsergebnisse
Abb.: Versuchsergebnisse
Aufgabe:
Entwerfen Sie für diesen Praktikumsversuch Arbeitsaufträge für Übungsaufgaben
mit Hilfe der unten stehenden Abbildung. Entnehmen Sie dazu Übungsinhalte aus
dem „Buddy Book“.
Thermolyse von Ammoniumchlorid: Herunterladen [docx] [201 KB]
