Klassenarbeit

 Untersuchung von Limonade und Zuckerwasser
Untersuchung von Limonade und Zuckerwasser
1. Erik möchte seine Lieblingslimonade untersuchen. Zuerst muss er das störende Kohlenstoffdioxid („Kohlensäure“) entfernen. Dazu stehen ihm folgende Laborgeräte zur Verfügung:
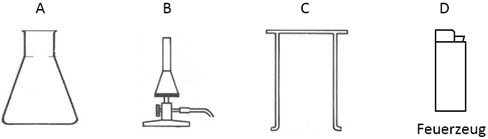
(C) Schnittzeichnung Laborgeräte:
Mit freundlicher Genehmigung des Bildungshauses Schulbuchverlage Westermann
Schroedel Diesterweg Schöningh Winklers GmbH, Georg-Westermann-Allee 66,
38104 Braunschweig
a)
Benenne die Laborgeräte A, B und C.
b)
Beschreibe, wie man vorgehen muss, um das Kohlenstoffdioxid aus der Limonadenprobe zu entfernen.
c)
Gib an, aufgrund welcher Eigenschaft von Kohlenstoffdioxid diese Methode funktioniert.
2. Nach Abkühlen auf Zimmertemperatur untersucht Erik die Limonade weiter.
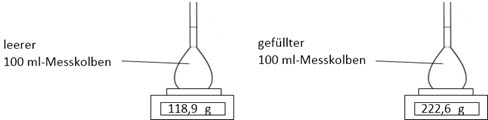
(C) Schnittzeichnung Laborgeräte: Mit freundlicher Genehmigung des Bildungshauses Schulbuchverlage Westermann Schroedel Diesterweg Schöningh Winklers GmbH, Georg-Westermann-Allee 66, 38104 Braunschweig
a)
Berechne die Dichte der „kohlenstoffdioxidfreien“ Limonade.
b)
Erik erhält die Dichte 2,226 g/ml. Erläutere, was er falsch gemacht hat.
Erik findet im Internet die folgende Tabelle:
|
Dichte von Zuckerwasser |
1,000 g/cm³ |
1,017 g/cm³ |
1,034 g/cm³ |
1,053 g/cm³ |
1,071 g/cm³ |
|
100 ml davon enthalten… |
…0g
|
…5g
|
…10g
|
…15g
|
…20g
|
c) Bestimme mithilfe dieser Tabelle die Menge an Zucker, die ein Glas (200 mL) von Eriks Lieblingslimonade ungefähr enthält.
3.
Laura stellt Zuckerwasser her, das viel süßer ist als die Limonade von Erik. Dazu vermischt sie 100 ml Wasser mit 100 g Zucker und rührt so lange, bis kein Zucker mehr sichtbar ist.
Gib an, was mit dem Zucker passiert ist und warum man ihn nicht mehr sehen kann.
4. Laura hat die Vermutung, dass der viele Zucker die Siedetemperatur verändert. Daher baut sie eine Apparatur auf, mit der sie die Siedetemperatur des Zuckerwassers bestimmen kann.
a)
Gib an, welche Laborgeräte sie außer A, B, C und D hierzu benötigt
b)
Zeichne eine beschriftete Versuchsskizze.
Bei der Messung der Siedetemperatur ergibt sich die folgende Tabelle
|
Zeit in Minuten |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
Temperatur in °C |
20 |
30 |
45 |
64 |
73 |
88 |
95 |
101 |
102 |
102 |
c)
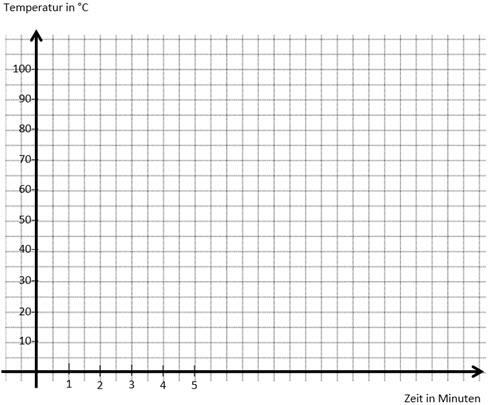
Erstelle aus den Wertepaaren der Tabelle ein Punktdiagramm.
d)
Führe das Diagramm für weitere zwei Minuten fort.
e)
Lies aus dem Diagramm die Siedetemperatur des Zuckerwassers ab.
5. Laura verrät Max nicht, wieviel Zucker sie für ihr Zuckerwasser verwendet hat. Sie gibt ihm aber 50 ml davon und fordert ihn auf: „Krieg’s doch raus!“
Max möchte den Zucker mit Filterpapier aus dem Zuckerwasser „herausfiltern“ und führt ein entsprechendes Experiment durch.
a)
Begründe, ob diese Methode hier funktioniert.
b)
Gib an, was bei dieser Filtration das Filtrat bzw. der Filterrückstand ist.
6. Nun versucht Max sein Glück mit einer Destillation.
a)
Erkläre, welcher Fehler sich in diese Versuchsskizze eingeschlichen hat.
b)
Erkläre, warum dieser Fehler in diesem Fall keine Auswirkung hat.
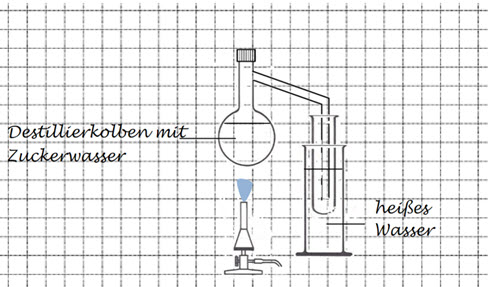
(C) Schnittzeichnung Laborgeräte: Mit freundlicher Genehmigung des Bildungshauses Schulbuchverlage Westermann Schroedel Diesterweg Schöningh Winklers GmbH, Georg-Westermann-Allee 66, 38104 Braunschweig
c) Ergänze den Lückentext:
Das Zuckerwasser wird im Destillierkolben _____________________, bis es nach einiger Zeit anfängt zu __________________. Nun _______________________ ständig Wasser. Der Wasserdampf gelangt in das seitliche Rohr, kühlt in der ____________________________ ab und ________________________. In dem Rohr bilden sich ______________________________, die langsam herunterlaufen und sich in dem Reagenzglas sammeln.
Leider funktioniert diese Methode nicht, denn nach einiger Zeit entsteht ein dicker, brauner Sirup der schließlich bei der Hitze verkohlt! Schade!
Klassenarbeit: Herunterladen [docx] [568 KB]
Klassenarbeit: Herunterladen [pdf] [668 KB]
Weiter zu Lösungen zu den Klassenarbeitsaufgaben
