Zellspannung galvanischer Elemente
Infobox
Diese Seite ist Teil einer Materialiensammlung zum Bildungsplan 2004: Grundlagen der Kompetenzorientierung. Bitte beachten Sie, dass der Bildungsplan fortgeschrieben wurde.
An Ihrem Arbeitsplatz haben Sie bereits eine Zinkhalbzelle und eine Kupferhalbzelle.
Zusätzlich erhalten Sie noch zwei weitere Bechergläser mit folgenden Halbzellen:
Silber in Silbernitratlösung (c = 0,1 mol·L
-1
) Ag/Ag
+
Eisen in Eisensulfatlösung (c = 0,1 mol·L
-1
) Fe/Fe
2+
Aufgabe:
Schreiben Sie alle möglichen Kombinationen von Halbzellen zu galvanischen Zellen in der folgenden Tabelle auf und ermitteln Sie experimentell deren Zellspannungen:
| Galvanisches Element | Zellspannung U z in V |
| Zn/Zn 2+ //Cu 2+ /Cu | 1,1 |
Stellen Sie die Zellspannungen grafisch dar. Ergänzen Sie damit die bereits vorbereitete Darstellung der Zellspannung der Zink-Kupfer-Zelle.
(Tragen Sie zum Beispiel die Zellspannung einer galvanischen Zelle, in der ein anderes Metall als Minuspol mit der Kupferhalbzelle kombiniert ist, in entsprechendem Maßstab von Cu/Cu
2+
nach links wie angedeutet ab usw.)
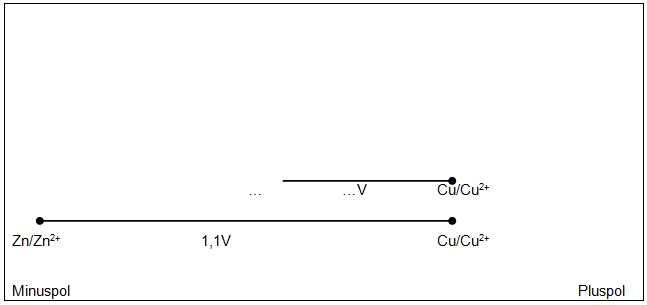
Zusatzaufgabe:
Erklären Sie mit Hilfe der Graphik, wie man mit Kenntnis der Zellspannungen einiger galvanischer Elemente unbekannte Zellspannungen rechnerisch ermitteln kann.
Zellspannung galvanischer Elemente: Herunterladen [doc] [57 KB]
Zellspannung galvanischer Elemente: Herunterladen [pdf] [84 KB]
