Lehrerinformation
Infobox
Diese Seite ist Teil einer Materialiensammlung zum Bildungsplan 2004: Grundlagen der Kompetenzorientierung. Bitte beachten Sie, dass der Bildungsplan fortgeschrieben wurde.
Hinweis
Es wird darauf hingewiesen, dass für jedes Experiment entsprechend der eigenen Durchführung vor der erstmaligen Aufnahme der Tätigkeit eine Gefährdungsbeurteilung durchgeführt und dokumentiert werden muss. Jede fachkundige Nutzerin/jeder fachkundige Nutzer muss die aufgeführten Inhalte eigenverantwortlich prüfen und an die tatsächlichen Gegebenheiten anpassen.
Weder die Redaktion des Lehrerfortbildungsservers noch die Autorinnen und Autoren der veröffentlichten Experimente übernehmen jegliche Haftung für direkte oder indirekte Schäden, die durch exakten, veränderten oder fehlerhaften Nachbau und/oder Durchführung der Experimente entstehen. Weiterführende Informationen erhalten Sie unter www.gefahrstoffe-schule-bw.de
INFO
Bei den hier angeführten Versuchen wird das Permanganat-Ion zu unterschiedlichen, jedoch bei einzelnen Versuchen wiederkehrend gleichen Oxidationsstufen reduziert. Die drei hier angeführten Versuche können daher alternativ alle nacheinander oder auch wahlweise einzeln im Praktikum durch-geführt werden.
Versuch 1: Oxidation primärer und sekundärer Alkohole
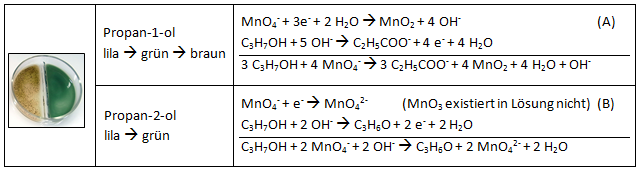
Bei der Oxidation von 1-Propanol können auch – entsprechend den Beobachtungen – zwei Gleichungen für die schrittweise Reduktion des Kaliumpermanganats aufgestellt werden. Quelle: http://www.axel-schunk.de/experiment/edm0799.html (verändert)
Versuch 2: Redoxreaktionen „mit Gummibärchen“
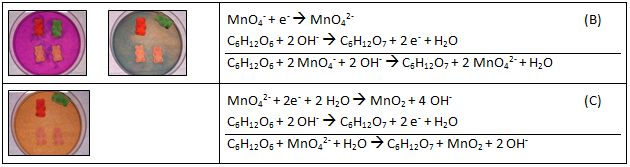
Quelle: http://fss.plone.uni-giessen.de/fss/fbz/fb08/Inst/Chemiedidaktik/mat/dat/gum.pdf/file/Gummibaerchen_Skript.pdf (verändert)
Versuch 3: Reduktion von Kaliumpermanganat bei unterschiedlichen pH-Werten

Führt man den Versuch mit Natriumthiosulfatlösung statt mit Natriumsulfitlösung durch, so beobachtet man im ersten Schalendrittel nach der anfänglichen Entfärbung nach einiger Zeit eine milchige Trübung.
| MnO 4 - + 5 e - + 8 H 3 O + | → Mn 2+ + 12 H 2 O | (D) |
| 2 S 2 O 3 2- | → S 4 O 6 2- + 2 e - | (E) |
2 MnO 4 - + 16 H 3 O+ + 10 S 2 O 3 2- → 2 Mn 2+ + 24 H 2 O + 5 S 4 O 6 2-
Im
Sauren
reagiert noch vorhandenes Natriumthiosulfat (Überschuss!) in einer Disproportionierungsreaktion zu Schwefeldioxid und Schwefel:
S
2
O
3
2-
+ 2 H
3
O
+
→ 3 H
2
O + SO
2
+ S
Quelle: http://www.axel-schunk.de/experiment/edm0504.html (verändert)
Lehrerinformation: Herunterladen [doc] [501 KB]
Lehrerinformation: Herunterladen [pdf] [317 KB]
