Diagnose
Infobox
Diese Seite ist Teil einer Materialiensammlung zum Bildungsplan 2004: Grundlagen der Kompetenzorientierung. Bitte beachten Sie, dass der Bildungsplan fortgeschrieben wurde.
Was kannst du (schon)?
- Falte zunächst das Blatt entlang des Pfeils nach hinten.
- Mache Dir zunächst alleine Gedanken über Deine Fähigkeiten und kreuze an.
- Tausche Dich im Folgenden mit Deinem Nachbar aus bzw. falte das Blatt auf, um die Fördermaßnahmen zu sehen. Weitergehend kannst du auch andere Mitschüler oder den Lehrer befragen.
|
Ich kann … |
sicher |
zieml. sicher |
unsicher |
sehr unsicher |
Schau nach |
|
|
1 |
beschreiben, was man unter der Organischen Chemie versteht. |
|
|
|
|
S. 231f |
|
2 |
einen Versuch erklären, mit dem man die Bausteine C und H in einer Verbindung nachweisen kann. |
|
|
|
|
S. 233 |
|
3 |
einen Versuch beschreiben, mit dem man Kohlenstoffdioxid nachweisen kann. |
|
|
|
|
S. 235 |
|
4 |
die Reaktionsgleichung für den Nachweis von Kohlenstoffdioxid formulieren. |
|
|
|
|
S. 235 |
|
5 |
erklären, wie Erdöl und Erdgas entstehen. |
|
|
|
|
S. 238f |
|
6 |
einen Versuch zur Bestimmung der molaren Masse von Gasen beschreiben. |
|
|
|
|
AB |
|
7 |
einen Versuch zur Bestimmung der molaren Masse von Gasen auswerten. |
|
|
|
|
AB |
|
8 |
eine Definition einer homologen Reihe angeben. |
|
|
|
|
AB
|
|
9 |
erklären, was man unter "Isomeren" versteht. |
|
|
|
|
S .242 |
|
10 |
aus der Strukturformel des jeweiligen Alkanmoleküls den Namen des Alkans ableiten. |
|
|
|
|
AB
|
|
11 |
ausgehend vom Namen eines Alkans die Strukturformel des jeweiligen Moleküls angeben. |
|
|
|
|
AB
|
|
12 |
stöchiometrische Berechnungen anhand von Reaktionsgleichungen durchführen. |
|
|
|
|
Heft |
|
13 |
die verschiedenen Arten der Zwischenmolekularen Kräfte erklären. |
|
|
|
|
AB
|
|
14 |
anhand der Strukturformel von Alkanmolekülen die Siedetemperatur des jeweiligen Stoffes vergleichend abschätzen. |
|
|
|
|
S. 244 |
|
15 |
ein Gaschromatogramm auswerten. |
|
|
|
|
Heft |
Alle Seitenangaben beziehen sich auf elemente chemie 1, Klett 2007
Aufgaben
1) Definiere, was man unter der Organischen Chemie versteht. (1)
2) Erkläre, wie Erdöl bzw. Erdgas entstehen. (5)
3) Es werden jeweils ein Liter Methan bzw. Butan verbrannt.
- Gib die Reaktionsgleichungen für die Verbrennungen an. (2)
- Beschreibe jeweils ein Experiment zum Nachweis der Reaktionsprodukte.(2, 3)
- Wie viel Liter Sauerstoff werden jeweils für die Verbrennung benötigt bzw. wie viel Liter Kohlenstoffdioxid entstehen? (12)
4) 120 ml eines Gases, das nur aus C und H aufgebaut ist, haben bei Raumtemperatur eine Masse von 150 mg.
- Beschreibe einen Versuchsaufbau, mit dem man zu den obigen Versuchsergebnissen kommen kann. (6)
- Ermittle die Masse bzw. Summenformel der Moleküle des Gases. (7)
5)
-
Gib die Halbstrukturformeln für die Moleküle der folgenden Verbindungen an: (11)
- 3,3-Dimethylhexan2-Methylhexan
- 3-Ethylhexan
- 3-Ethyl-2-methylpentan
- 2,3,4-Trimethylhexan
- Welche sind isomer zueinander?
6) Gib die Strukturformel der Moleküle der folgenden Stoffe an und ordne diesen die folgenden Siedetemperaturen zu. Begründe Deine Zuordnung. (10, 13, 14)
n-Pentan, Wasser, 2,2-Dimethylpropan; 100°C, 9°C, 36°C
7) Gib die Strukturformeln aller Isomere, der Summenformel C6H14 an und benenne diese. (9, 10)
8)
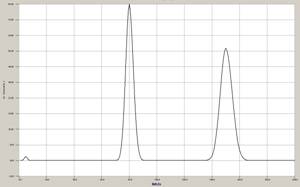 Bei der gaschromatografischen Analyse eines Kohlenwasserstoff-Gemischs ergibt sich das nebenstehende Gaschromatogramm. (15)
Bei der gaschromatografischen Analyse eines Kohlenwasserstoff-Gemischs ergibt sich das nebenstehende Gaschromatogramm. (15)
- Beschreibe den Versuchsaufbau und das Funktionsprinzip eines Gaschromatografen.
- Erkläre, wie viele Komponenten das Gemisch mindestens enthält.
- Erläutere, wie sich die prozentuale Zusammensetzung des Gemisches ermitteln lässt.
9) Bei der Verbrennung eines Stoffes dessen Moleküle aus C- und H-Atomen aufgebaut ist, entstehen (lässt man die Reaktionsprodukte auf Raumtemperatur abkühlen), 72 L Kohlenstoffdioxid und 72 g Wasser.
- Ermittle die Summenformel. (12)
- Mache einen Vorschlag für die Strukturformel.
Diagnose: Herunterladen [doc] [595 KB]
Diagnose: Herunterladen [pdf] [377 KB]
Rätsel: Herunterladen [doc] [79 KB]
Rätsel: Herunterladen [pdf] [118 KB]
