Aufgaben
Infobox
Diese Seite ist Teil einer Materialiensammlung zum Bildungsplan 2004: Grundlagen der Kompetenzorientierung. Bitte beachten Sie, dass der Bildungsplan fortgeschrieben wurde.
zum Thema „Säuren und Basen“:
- Gib die Definition einer Säure bzw. Base nach Brønsted an.
- Notiere die Reaktionsgleichung für die Reaktion von Ammoniak mit Chlorwasserstoff. Ordne den Teilchen die Begriffe Säure und Base zu.
-
Bei welchen Reaktionen handelt es sich um Säure-Base-Reaktionen? Gib gegebenenfalls an, welche Teilchen als Säure, welche als Base reagieren.
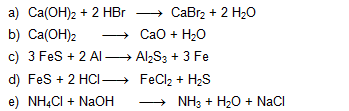
-
Löst man Chlorwasserstoff-Gas in Wasser, so entsteht eine saure Lösung.
Löst man Ammoniak-Gas in Wasser entsteht eine alkalische Lösung.- Schreibe für die beiden ablaufenden Vorgänge jeweils eine Reaktionsgleichung und erkläre anhand dieser die Bildung einer sauren bzw. alkalischen Lösung.
- Erkläre, weshalb bei beiden Vorgängen die elektrische Leitfähigkeit der Lösungen zunimmt.
- Gib ein Beispiel für eine Neutralisationsreaktion an und schreibe für den Neutralisationsvorgang eine Reaktionsgleichung.
- Beschreibe mit eigenen Worten, was man unter der Stoffmengenkonzentration versteht.
- Skizziere einen beschrifteten Versuchsaufbau für eine Säure-Base-Titration.
-
Bei der Titration von 5 ml einer unbekannten alkalischen Lösung mit Salzsäure der Konzentration c = 0,1 mol/L werden bis zum Neutralpunkt 18,4 ml Salzsäure verbraucht.
- Berechne die Konzentration der verwendeten alkalischen Lösung.
- Gib an, auf welche Teilchen sich die gemachte Konzentrationsangabe bezieht.
Säure:
Herunterladen
[doc]
[54 KB]
Säure:
Herunterladen
[pdf]
[131 KB]
